



薬理学分野による研究成果が「Neurochemistry International」誌に掲載されました
2022.03.01
本学薬学科の薬理学分野(中西 博 教授、野中 さおり 講師)と長崎大学との共同研究成果「Secreted gingipains from Porphyromonas gingivalis increase permeability in human cerebral microvascular endothelial cells through intracellular degradation of tight junction proteins 」が「Neurochemistry International」誌に掲載されました。(doi: 10.1016/j.neuint.2022.105282)
歯周病は、30~50歳代で約8割、60歳代では約9割と非常に罹患率が高い疾患です。近年、歯周病の病原性は歯周組織のみに留まらず、アルツハイマー型認知症の増悪因子となることがわかってきました。その仕組みとしては、歯周病菌やその病原性因子がもろくなった歯肉の血管に入って全身に運ばれ、脳へと移行して神経細胞死の原因となる脳内炎症を引き起こすためだと考えられています。しかし、脳の血管は、それを構成する内皮細胞どうしが密着結合で強固に結合することでバリアを作り、細菌を含む有害物の脳への移行を制限しています。歯周病菌やその病原性因子がこのバリアを通過して脳へと移行する仕組みについては不明でした。
本論文では、代表的な歯周病菌のジンジバリス菌が分泌するタンパク質分解酵素「ジンジパイン」が密着結合を構成するタンパク質を直接分解することで、脳血管バリアを壊しその透過性を上げることを明らかにしました。さらに、この時、ジンジパインは、ジンジバリス菌が分泌する外膜小胞(outer membrane vesicle (OMV))に結合した状態で脳血管内皮細胞内に侵入し、細胞の内側から密着結合構成タンパク質を分解することを突き止めました。
ジンジパインによる脳血管バリアの破綻を防ぐことができれば、歯周病菌が脳に侵入できなくなり、歯周病によるアルツハイマー型認知症の発症・増悪が止められる可能性があります。従って、本研究の成果は、OMV上のジンジパインを標的にした薬や、OMV分泌阻害薬など、アルツハイマー型認知症に対する予防・治療薬の開発に貢献することが期待できます。
参考: Saori Nonaka, Tomoko Kadowaki, Hiroshi Nakanishi. Neurochem. Int., 154, 105282, 2022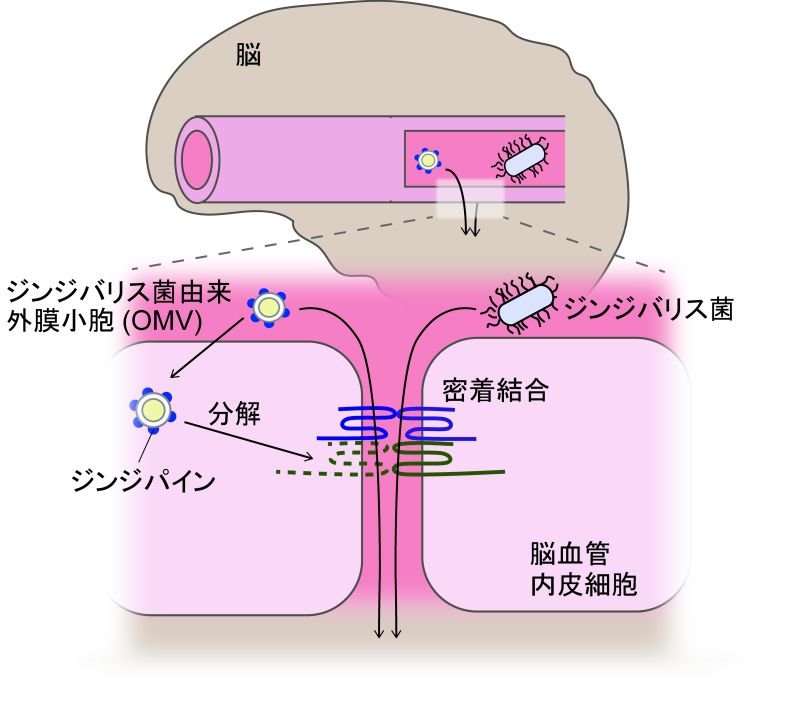
歯周病菌が分泌するジンジパインによる脳血管バリア破綻の仕組み